Un paziente di 54 anni affetto da cardiomiopatia dilatativa a coronarie indenni, portatore di defibrillatore con terapia di resincronizzazione cardiaca (CRT-D), è giunto alla nostra osservazione per comparsa negli ultimi mesi di episodi di stimolazione diaframmatica. È un paziente con multipli fattori di rischio cardiovascolare e un’insufficienza renale di stadio 3b. 7 anni prima, in considerazione dello sviluppo di blocco di branca sinistra e della severa dilatazione del ventricolo sinistro con importante riduzione della frazione di eiezione (Vol td/ts 286/201 ml; FE 30%) nonostante terapia medica massimale, era stato sottoposto a impianto di CRT-D con elettrocatetere bipolare per il ventricolo sinistro, con beneficio sulla sintomatologia e rimodellamento inverso del ventricolo sinistro (FE 42%, Vol td/ts 221/129 ml).
Da alcuni mesi il paziente riferiva la comparsa di stimolazione diaframmatica incostante e variabile nelle diverse posizioni. All’interrogazione del device si è osservato un abbassamento della soglia del nervo frenico, probabilmente legata all’evoluzione della malattia, con progressione del rimodellamento ventricolare e aumento della dilatazione ventricolare sinistra. È stato effettuato un test nelle configurazioni disponibili con riscontro di riduzione della soglia del nervo frenico (2 mV @0,4 ms) e rialzo della soglia muscolare (1,3 mV @0,4ms). È stato riprogrammato il device nella miglior configurazione, con stimolazione catodica con uscita 1,75 mV @0,4 ms.
In considerazione della persistenza di sintomatologia e dell’impossibilità di gestire conservativamente il problema, si è deciso di procedere a posizionare un nuovo elettrocatetere. Per valutare la pervietà degli accessi venosi è stata eseguita la venografia con CO2, per minimizzare l’utilizzo del mezzo di contrasto alla luce dell’insufficienza renale cronica. Alla venografia vi era un’ostruzione della vena succlavia fino alla vena anonima con formazione di circoli collaterali. (Figura 1).
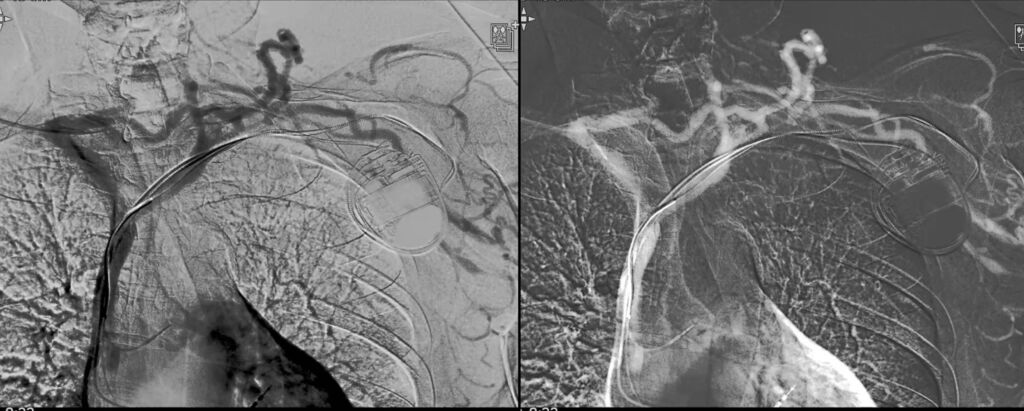
Figura 1. Venografia dell’asse axillo-succlavio con anidride carbonica (CO2). Si osserva un’ostruzione della vena succlavia fino alla vena anonima con formazione di circoli collaterali.
Per via di tale ostruzione è stata valutata l’opzione di eseguire l’impianto di un elettrodo leadless endocardico per il ventricolo sinistro (WISE-CRT), tuttavia l’ostruzione era localizzata per cui si è deciso di eseguire una puntura diretta della vena anonima a valle dell’ostruzione sotto guida ecografica, con successivo controllo radioscopico (Figura 2).
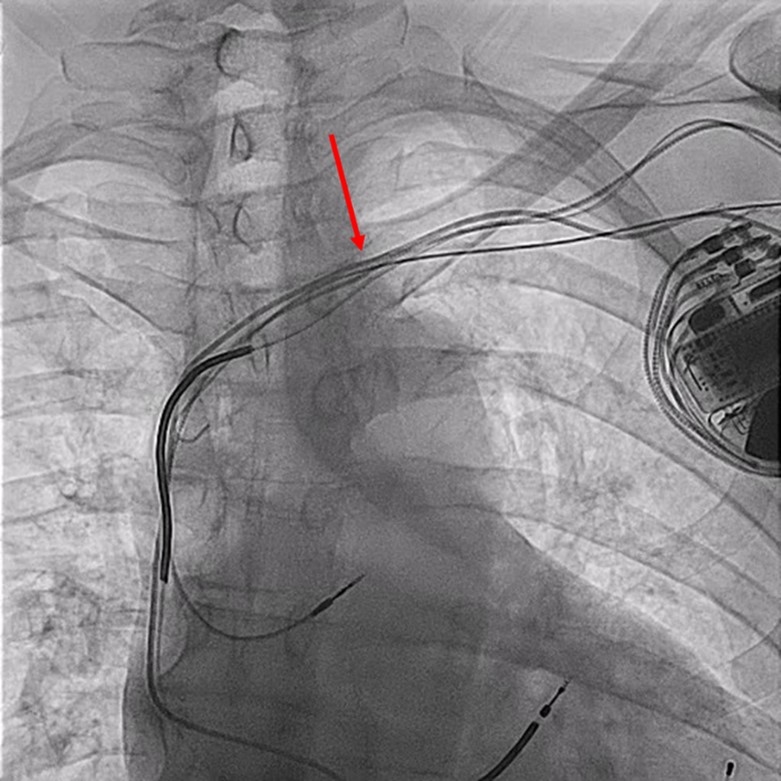
Figura 2. Controllo radioscopico dopo puntura diretta della vena anonima a valle dell’ostruzione della vena succlavia.
Dopo cannulazione del seno coronarico con guida idrofilica e posizionamento del delivery in seno coronarico è stata eseguita una venografia selettiva: vena laterale con ingresso angolato e stenosi severa. In assenza di un’adeguata vena target è stata valutata la possibilità di eseguire un impianto a livello hissiano, tuttavia la cannulazione della vena laterale con sottoselettore e guida è risultata agevole e si è preferito effettuare un’angioplastica con impianto di stent del vaso al fine di ottenere rettilineizzazione e dilatazione del ramo (Figura 3).
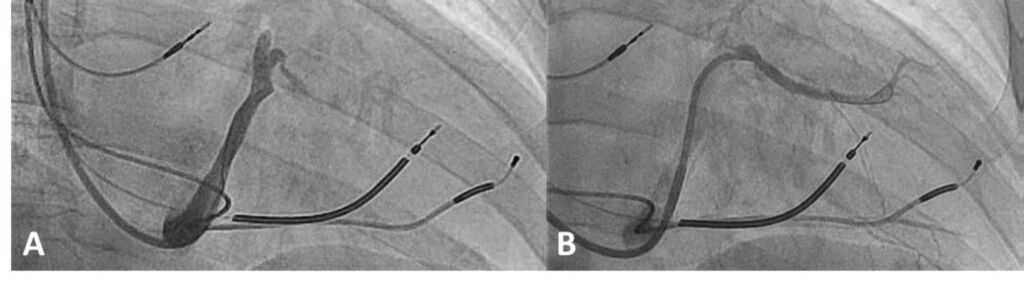
Figura 3. A. Venografia selettiva del seno coronarico: vena laterale con ingresso angolato e stenosi severa. B. Angioplastica con impianto di stent della vena laterale.
Visto il rischio di dislocazione e la necessità di stimolare la porzione medio ventricolare è stato posizionato un catetere quadripolare a fissazione attiva. L’elettrocatetere è stato tunnellizzato dalla puntura distale dell’anonima fino alla tasca del generatore. La stimolazione finale è stata programmata LV2->LV3 con soglia 0.75V @0.4ms e assenza di stimolazione del nervo frenico anche ad elevati voltaggi (Figura 4).
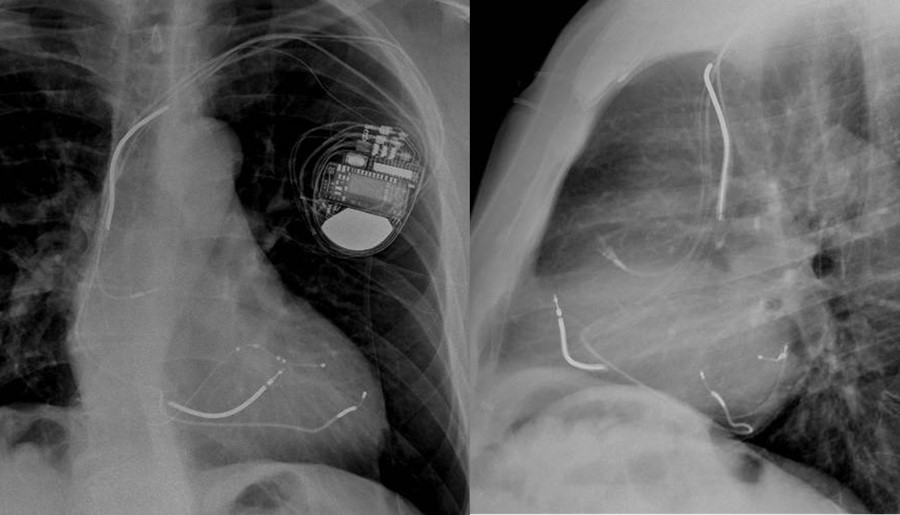
Figura 4. RX torace antero-posteriore e latero-laterale eseguito dopo l’impianto.
DISCUSSIONE
Questo caso clinico offre la possibilità di evidenziare diverse strategie adottabili per offrire una resincronizzazione cardiaca e per superare alcuni fattori limitanti come la presenza di un’ostruzione venosa, un’anatomia delle vene coronariche non favorevole o una difficile gestione della stimolazione frenica.
L’ostruzione o la stenosi della vena succlavia e/o anonima è un’evenienza frequente nei pazienti portatori di dispositivo, tanto da interessare fino al 30% dei soggetti portatori di device. Nei pazienti che devono essere sottoposti ad up-grade è quindi importante andare a valutare la pervietà del sistema venoso. L’utilizzo della CO2 come alternativa ai mezzi di contrasto iodati si è diffusa principalmente nel distretto arterioso, ma si sta affermando anche a livello venoso grazie al suo profilo di sicurezza, in particolare nei soggetti con allergia al mezzo di contrasto ed insufficienza renale. 1
In letteratura sono descritte diverse strategie di impianto/up-grade che possono essere attuate in caso di ostruzione della vena succlavia, tra cui ricorrere ad un impianto controlaterale, oppure procedere alla ricanalizzazione del vaso mediante estrazione dei cateteri presenti o attraverso procedure di venoplastica. In questo caso il tipo di ostruzione offriva la possibilità di ricorrere ad un accesso mediale all’ostruzione, che grazie all’utilizzo di una guida ecografica può essere condotto in condizioni di sicurezza. 2,3
Per quanto riguarda l’anatomia non favorevole delle vene coronariche, dovuta ad una vena laterale con ingresso angolato e stenosi severa, si è optato per l’angioplastica con posizionamento di stent. L’angioplastica delle vene coronariche si è rivelata una tecnica efficace e sicura per facilitare il posizionamento degli elettrocateteri in caso di stenosi delle vene target.4 L’utilizzo di stent a livello delle vene coronariche è nato come procedura di “salvataggio” per prevenire il tamponamento cardiaco in caso alla dissezione accidentale o iatrogena del seno coronarico o dei suoi rami, tuttavia l’impianto di stent si è rivelato utile nel fissaggio dei cateteri a livello delle vene coronariche e dopo angioplastica delle vene coronariche per superare stenosi e rettilineizzare i vasi. 5
La resincronizzazione cardiaca non si limita però all’esecuzione di un impianto biventricolare con posizionamento di un elettrocatetere per il ventricolo sinistro. La stimolazione del tessuto di conduzione, sia a livello del fascio di His che della branca sinistra, si è dimostrata una strategia fattibile ed efficace a lungo termine, con effetti simili a quelli della convenzionale stimolazione biventricolare e deve essere considerata come valida alternativa. 6–9 A ciò si aggiunge la possibilità di eseguire l’impianto di un elettrodo leadless endocardico per il ventricolo sinistro (WISE system). Questo approccio permette di superare i limiti legati all’ostruzione degli accessi venosi e allo stesso tempo garantisce una stimolazione endocardicaior possibilità di scegliere un sito con attivazione meccanica tardiva e non interessato da fibrosi. 10,11
La strategia di resincronizzazione cardiaca deve pertanto essere personalizzata sul paziente, sfruttando tutte le diverse strategie per offrire la soluzione adatta, minimizzando i rischi e le possibili complicanze della procedura.
BIBLIOGRAFIA
1. Winters SL, Curwin JH, Sussman JS, et al. Utility and Safety of Axillo-subclavian Venous Imaging with Carbon Dioxide (CO2) Prior to Chronic Lead System Revisions: CARBON DIOXIDE CONTRAST VENOGRAPHY. Pacing Clin Electrophysiol 2010;33(7):790–4.
2. Burri H. Overcoming the challenge of venous occlusion for lead implantation. Indian Pacing Electrophysiol J 2015;15(2):110–2.
3. Antonelli D, Freedberg NA, Turgeman Y. Supraclavicular vein approach to overcoming ipsilateral chronic subclavian vein obstruction during pacemaker-ICD lead revision or upgrading. Europace 2010;12(11):1596–9.
4. Yi F, Wu F, Shen M, et al. Coronary vein angioplasty to facilitate implantation of left ventricular lead. Europace 2010;12(11):1600–3.
5. Niazi I, Bajwa T, Sra J, Akhtar M. A Review of Innovative Strategies for CRT Implantation: Part II — Coronary Venous Stenting. J Innov Card Rhythm Manag 2011;6.
6. Abdelrahman M, Subzposh FA, Beer D, et al. Clinical Outcomes of His Bundle Pacing Compared to Right Ventricular Pacing. J Am Coll Cardiol 2018;71(20):2319–30.
7. Upadhyay GA, Vijayaraman P, Nayak HM, et al. On-treatment comparison between corrective His bundle pacing and biventricular pacing for cardiac resynchronization: A secondary analysis of the His-SYNC Pilot Trial. Heart Rhythm 2019;16(12):1797–807.
8. Wu S, Su L, Vijayaraman P, et al. Left Bundle Branch Pacing for Cardiac Resynchronization Therapy: Nonrandomized On-Treatment Comparison With His Bundle Pacing and Biventricular Pacing. Can J Cardiol 2021;37(2):319–28.
9. Chen X, Ye Y, Wang Z, et al. Cardiac resynchronization therapy via left bundle branch pacing vs. optimized biventricular pacing with adaptive algorithm in heart failure with left bundle branch block: a prospective, multi-centre, observational study. EP Eur 2021;euab249.
10. Sidhu BS, Sieniewicz B, Gould J, et al. Leadless left ventricular endocardial pacing for CRT upgrades in previously failed and high-risk patients in comparison with coronary sinus CRT upgrades. Eur Eur Pacing Arrhythm Card Electrophysiol J Work Groups Card Pacing Arrhythm Card Cell Electrophysiol Eur Soc Cardiol 2021;23(10):1577–85.
11. Sieniewicz BJ, Betts TR, James S, et al. Real-world experience of leadless left ventricular endocardial cardiac resynchronization therapy: A multicenter international registry of the WiSE-CRT pacing system. Heart Rhythm 2020;17(8):1291–7.