Un piccolo problema
Il caso clinico riguarda una paziente di 80 anni, ipertesa, diabetica ID, dislipidemica, obesa.
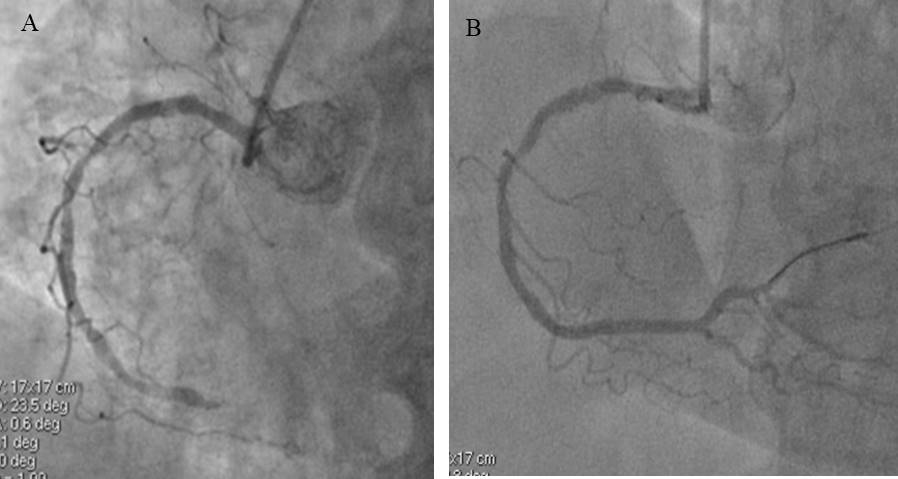
In anamnesi riferite pregresse ischemie cerebrali con residua ipomobilità agli arti inferiori. Da qualche tempo episodi di dolore toracico intermittente con progressiva ingravescenza della sintomatologia. Per un nuovo e prolungato episodio di dolore toracico associato a sudorazione algida veniva accompagnata tramite 118 al PS. All’ECG evidenza di STEMI inferiore, motivo per cui veniva inviata d’urgenza in sala di emodinamica e veniva trattata con angioplastica primaria sulla coronaria destra con impianto di uno stent medicato alla crux (Figura 1, panel A e B). All’ecocardiogramma riscontro di funzione contrattile globale depressa (FE 45%) con ipocinesia laterale, acinesia inferiore e posteriore, insufficienza mitralica moderata.
La comparsa di fibrillazione atriale post-procedurale richiedeva il trattamento antiaritmico farmacologico (amiodarone). Pertanto al fine di risparmiare il patrimonio venoso periferico, già scarso, della paziente veniva richiesto il posizionamento di un PICC.
La procedura d’impianto risultava più difficoltosa del previsto per l’impossibilità di avanzare il filo guida dedicato oltre la vena ascellare dx. Nel tentativo di mantenere l’accesso venoso, evitando una nuova puntura ecoguidata della vena basilica (anche alla luce della triplice terapia antitrombotica praticata) si è optato per uno switch tra PICC e Midline utilizzando come guida di scambio un filo guida coronarico da 0.014′. Durante le manovre di scambio si è osservata la comparsa di un run di tachicardia ventricolare non sostenuta con successiva comparsa di blocco di branca destro. La procedura di impianto di Midline si è conclusa “apparentemente” senza complicanze.
Qualche giorno dopo la paziente rientrava in sala di emodinamica per essere sottoposta a procedura di completamento di rivascolarizzazione del tratto medio di coronaria destra e dell’arteria discendente anteriore, ma alla prima iniezione di mdc si osservava la presenza di un lungo frammento di filo guida coronarico che giaceva con la parte floppy all’interno del ventricolo destro e con la parte stiff all’interno di una diramazione segmentaria dell’arteria polmonare destra (Figura 2, panel C).
Ricostruendo l’accaduto con il personale infermieristico del PICC Team si è dedotto che il filo guida di scambio tra PICC e Midline si era verosimilmente fratturato nello shaft (probabilmente perchè difettoso) ed era migrato dalla vena ascellare destra alle sezioni destre cardiache. Qui, probabilmente, la parte floppy si è raggomitolata nei recessi del ventricolo destro, mentre la parte stiff sulla spinta del flusso sanguigno è migrata in arteria polmonare.
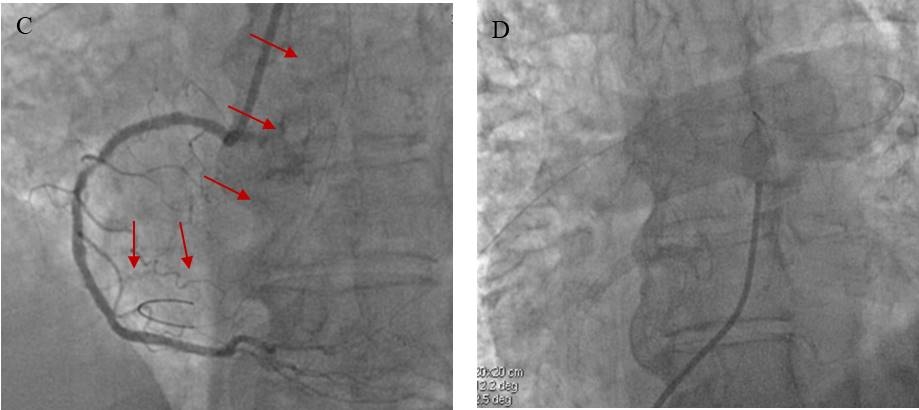
Dopo la procedura di completamento di rivascolarizzazione, si è proceduto al tentativo di cattura del corpo estraneo. Previa puntura ecoguidata della vena femorale è stata eseguita un’arteriografia polmonare per conferma della localizzazione del frammento di filo guida nelle sezioni destre (Figura 2, panel D).
Sono stati eseguiti numerosi tentativi con diverse tecniche per tentare di rimuovere il filo guida intrappolato.
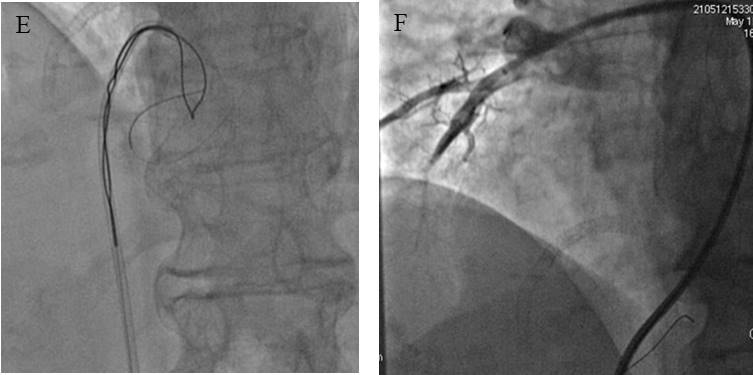
Inizialmente si è cercato di catturare l’estremità floppy con un cappio dedicato “MultiSnare” (Figura 3, panel E). Tuttavia ci si è ben presto resi conto che questa estremità era incarcerata tra le trabecole del Vdx, sotto il piano tricuspidalico. L’estremità stiff, invece, era localizzata in una piccola diramazione subsegmentaria dell’arteria polmonare destra che non avrebbe ospitato il nostro catetere 8Fr, neanche ricorrendo ad una estensione del catetere (Child in Mother) 5.5 Fr (Figura 3, panel F). Inoltre, anche nell’ipotesi di riuscire ad agganciare la parte stiff della guida, trascinarla via era una ipotesi da scartare in quanto avrebbe potuto lacerare il ramo dell’arteria polmonare.
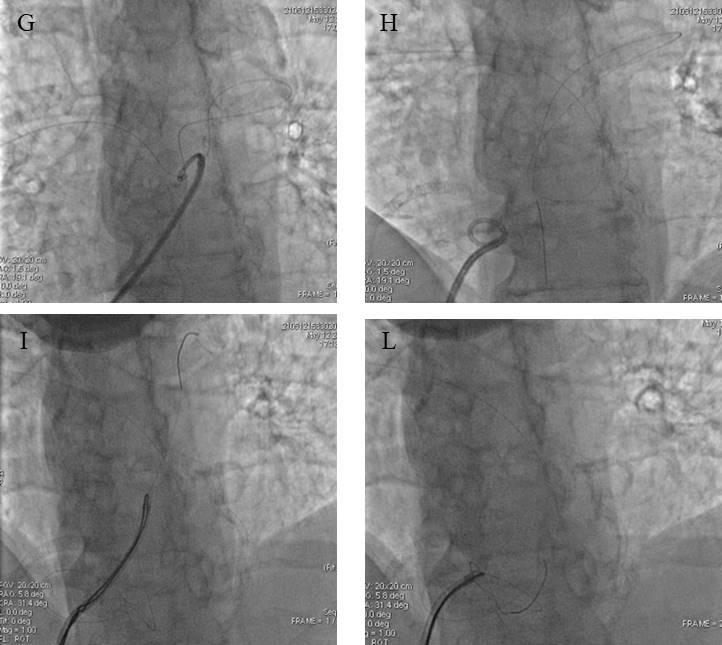
A questo punto si è deciso di cambiare strategia, cercando di “agguantare” la parte centrale della guida in modo da mobilizzarla nella speranza di trovare un appiglio. Il primo tentativo è stato quello di utilizzare una guida a ricciolo. Tuttavia l’impossibilità di manovrarla non consentiva di ottenere l’effetto desiderato. Sfruttando lo stesso principio è stato utilizzato un catetere PigTail 6Fr, il cui ricciolo è regolabile inserendovi una guida 0.35′ al suo interno. La possibilità di svolgere un’azione ad uncino con il catetere PigTail ha permesso di catturare il corpo della guida all’interno del tronco dell’arteria polmonare (Figura 4, panel G). Trascinando il PigTail in ventricolo destro abbiamo ottenuto l’effetto desiderato. In altre parole la parte stiff è rimasta ancorata al ramo dell’arteria polmonare, il corpo della guida ha formato un loop in ventricolo destro, mentre la parte floppy si è ribaltata in arteria polmonare sinistra. A questo punto il frammento di filo guida ha assunto una conformazione a Ɣ con l’estremità floppy libera in arteria polmonare sn (Figura 4, panel H). Il successivo passo ha previsto l’utilizzo di un cappio dedicato (MultiSnare) che ci ha permesso di ancorare la guida (Figura 4, panel I) al catetere trascinando tutto via (Figura 4, panel L).
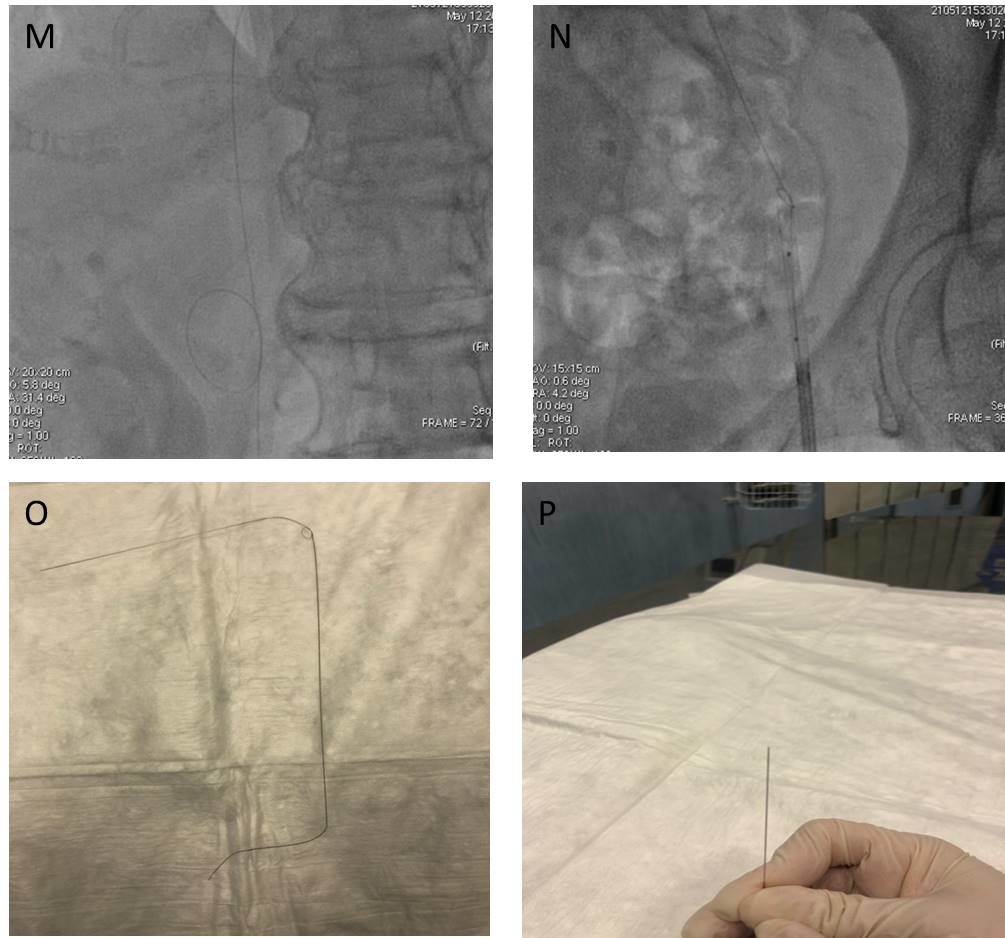
Durante la manovra di rimozione, la guida si è annodata su se stessa (figura 5, panel M) e tale nodo impediva la cattura della guida all’interno dell’introduttore venoso femorale. A questo punto si è deciso di utilizzare la tecnica del trapping con l’ausilio di un pallone che incarcerasse il sistema filo guida-cappio con il catetere e l’introduttore (figura 5, panel N). Quindi si è rimosso il tutto come un unico sistema (figura 5, panel O e P) e si è proceduto ad una emostasi venosa mediante compressiva manuale.
L’utilizzo di CVC, PICC e Midline negli ultimi anni è aumentato esponenzialmente. Sebbene si tratti di procedure a basso rischio di complicanze, la sempre crescente manualità degli operatori porta, in caso di necessità, ad utilizzare tecniche di cardiologia interventistica, e con esse le relative complicanze.
La rimozione di un frammento di filo guida è una complicanza temibile per l’alto rischio trombotico che ne deriva. La possibilità di rimozione attraverso materiali dedicati (cappi) prevede la presenza di un appiglio, in assenza del quale va creato con tutte le idee, i metodi e i materiali che si hanno a disposizione!