Se si vuole trovare qualcosa, non c’è niente di meglio che continuare a cercare
Un uomo di 67 anni si presenta a Novembre 2021 in Pronto Soccorso per palpitazioni, dolore toracico ed episodi di presincope. In anamnesi patologica remota si riporta recente diagnosi di Granulomatosi di Wegener, per cui esegue regolari controlli immunologici per interessamento del distretto orofaringeo; tra le altre comorbidità segnalate ateromasia carotidea e reflusso gastroesofageo. La terapia a domicilio è la seguente: Clopidogrel 75 mg/die, Prednisone 5 mg/die, Methotrexate 15 mg/sett., Folina 5 mg, Omeprazolo 20 mg/die, Risendronato 35 mg/sett., Pregabalin 25 mg x 2/die. Dal punto di vista cardiologico circa un anno prima gli accertamenti di base (ECG, ecocardiogramma ed ECG-Holter) risultavano nella norma.
All’ingresso in Pronto Soccorso si presentava con parametri vitali nella norma e in buon compenso di circolo emodinamico.
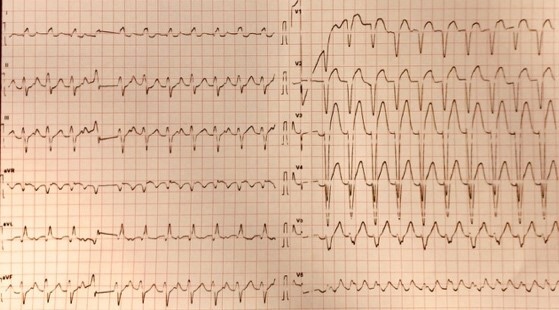
Figura 1: ECG a 12 derivazioni eseguito all’ingresso del paziente in Pronto Soccorso.
Veniva eseguito un elettrocardiogramma a 12 derivazioni (Figura 1), che evidenziava una tachicardia ventricolare monomorfa sostenuta, associata ad ipocinesia globale del ventricolo sinistro e frazione di eiezione moderatamente ridotta all’ecocardiografia transtoracica (TTE). Data la stabilità emodinamica, veniva trattato tempestivamente con amiodarone, con ripristino del ritmo sinusale (Figura 2).

Figura 2: ECG a 12 derivazioni successivo a cardioversione farmacologica con amiodarone, con ripristino di ritmo sinusale.
Trasferito nell’Unità della Terapia intensiva cardiologica, a distanza di un paio d’ore, si ripeteva l’ecocardiogramma transtoracico con regressione delle anomalie precedentemente evidenziate. Tuttavia, agli esami ematochimici risultava un marcato innalzamento della Troponina I (da 200 a 16456 ng/L), per cui veniva eseguita la coronarografia con esclusione di malattia coronarica sottostante. A questo punto la risonanza magnetica (RMN) cardiaca (Figura 3) evidenziava, dopo iniezione di mezzo di contrasto a base di Gadolinio, tessuto cicatriziale miocardico con pattern non ischemico in corrispondenza della parete media anterosettale basale, compatibile con esito miocarditico.
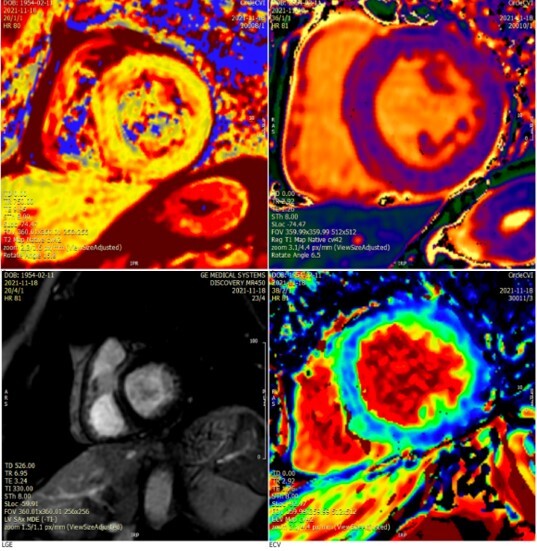
Figura 3: Risonanza magnetica cardiaca: Le sequenze TIR in pesatura T2 non mostrano chiare alterazioni patologiche. Normali valori del tempo T1. Normali valori del tempo T2. Normali valori di ECV. Le sequenze LGE mostrano stria di enhancement intramiocardico a livello del SIV anteriore basale (pattern non ischemico).
Durante lo studio elettrofisiologico (EPS), non è stata indotta nessuna aritmia ventricolare sostenuta anche con un protocollo aggressivo, e il mappaggio elettroanatomico di entrambi i ventricoli non ha mostrato alcun substrato aritmico. Successivamente è stato sottoposto ad impianto di defibrillatore (ICD) in prevenzione secondaria.
A distanza di 4 mesi, il paziente è stato nuovamente ricoverato per episodi multipli di TV sostenuta (con durata del ciclo nella finestra di monitoraggio ICD) refrattari ai farmaci ed a tre scariche da defibrillatore esterno. L’EPS ripetuto non è riuscito a indurre aritmie sostenute. Il mappaggio elettroanatomico ad alta densità del ventricolo destro, tuttavia, ha mostrato potenziali frammentati nella parete settale medio-posteriore (Figura 4).
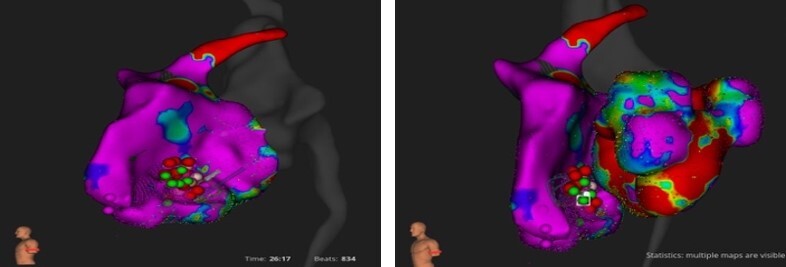
Figura 4: Ventricolo destro: Area di potenziali frammentati su SIV medio-posteriore, sulla quale si effettua biopsia endomiocardica mirata (2 prelievi, 3 frammenti di tessuto). Ventricolo sinistro: assenza di potenziali patologici.
Dopo la biopsia miocardica della suddetta regione, è stata eseguita l’ablazione transcatetere con radiofrequenza dell’area con regressione dei potenziali. I risultati della biopsia endomiocardica hanno dimostrato la fibrosi. A 12 mesi di follow-up, il paziente non ha più avuto recidive.
In conclusione, l’imaging multimodale è di fondamentale importanza nell’identificazione del substrato aritmogeno e nella caratterizzazione delle componenti anatomo-funzionali specifiche dei circuiti della TV. Nel nostro specifico caso, il mappaggio elettroanatomico ad alta densità è stato in grado di identificare potenziali frammentati e definire l’area target dell’ablazione, nonostante la discrepanza con la RMN.
Bibliografia:
(1) Santos LPS, Bomfim VG, Bezerra CF, Costa NV, Carvalho RBP, Carvalho RS, Passos
RDH, Boaventura OCB, Gobatto ALN. Heart conduction system defects and sustained
ventricular tachycardia complications in a patient with granulomatosis with polyangiitis. A
case report and literature review. Rev Bras Ter Intensiva. 2017 Jul-Sep;29(3):386-390.
(2) Gannon, M.P., Schaub, E., Grines, C.L. and Saba, S.G. (2019), State of the art: Evaluation and
prognostication of myocarditis using cardiac MRI. J. Magn. Reson. Imaging, 49: e122-e131
(3) 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the
prevention of sudden cardiac death: Developed by the task force for the management of
patients with ventricular arrhythmias and the prevention of sudden cardiac death of the
European Society of Cardiology (ESC) Endorsed by the Association for European Paediatric
and Congenital Cardiology (AEPC)
(4) Garg R, Friedrich MG. Cardiomyopathies. ESC CardioMed. 3rd ed. Oxford University
Press; 2022, p510–515
