Un uomo di origini pakistane di 32 anni, in follow up specialistico per tubercolosi extrapolmonare da coinvolgimento dei linfonodi mediastinici e con anamnesi cardiovascolare muta, si presenta in Pronto Soccorso per progressiva riduzione della tolleranza allo sforzo con dispnea ingravescente e dolore toracico di tipo oppressivo.
I parametri vitali sono stabili: PA 110/65 mmHg, FC 75 bpm, SpO2 97% in AA. L’esame obiettivo e gli esami strumentali di primo livello permettono di riscontrare segni di iniziale scompenso cardiaco destro, caratterizzato dalla presenza di edemi declivi improntabili con aumento della pressione venosa centrale, lieve iperbilirubinemia prevalentemente indiretta (totale 2 mg/dl), RX torace negativa per lesioni pleuro-parenchimali o segni di scompenso.
L’ECG si caratterizza per un ritmo sinusale normofrequente, bassi potenziali periferici e alterazioni della ripolarizzazione ventricolare a carattere aspecifico soprattutto a sede anteriore e inferiore (Figura 1). La curva troponinica permette di escludere sindromi coronariche acute (7 – 10 ng/L).

L’ecocardiogramma transtoracico (Figura 2) permette di apprezzare una massa intrapericardica, delle dimensioni di 60×40 mm e a contenuto disomogeneo, posta anteriormente al ventricolo destro con segni di compressione sullo stesso ed iniziali segni di ripercussione emodinamica (movimento paradosso del setto interventricolare, vena cava inferiore dilatata con ridotte escursioni respiratorie). La frazione di eiezione del ventricolo sinistro è conservata, non vi sono valvulopatie di rilievo.

Considerando la stabilità emodinamica del paziente, il contenuto sovrafluido della massa e di conseguenza la scarsa applicazione di un approccio percutaneo, dopo discussione collegiale in sede di Heart Team (cardiologo clinico, cardiologo interventista, cardiochirurgo), si propende per la rimozione chirurgica della massa in regime di urgenza.
Il paziente viene intanto sottoposto a esami strumentali di secondo livello per meglio caratterizzare la natura della massa con evidenza di:
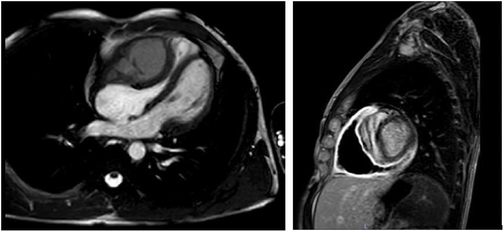
- RM cardiaca (Figura 3) con evidenza di versamento pericardico saccato adiacente alla parete libera del ventricolo destro, a contenuto sovrafluido (iperintenso in T1 e T2), delle dimensioni massime di 68x42mm. Diffusa impregnazione contrastografica precoce e tardiva dei foglietti pericardici, in rapporto a fenomeni flogistici. Compressione ab estrinseco del ventricolo destro che appare ridotto di volume ma con cinetica globale conservata.
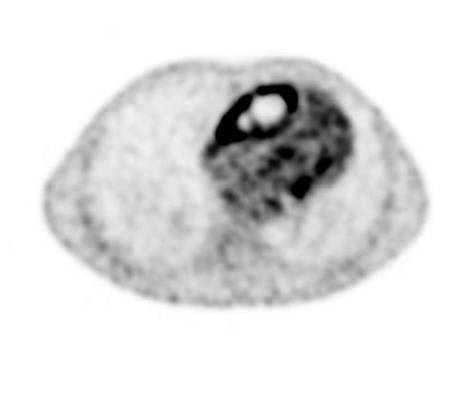
- PET TB con FDG (Figura 4) evidenza di intensa ipercaptazione a distribuzione periferica in corrispondenza del versamento pericardico saccato (SUVmax = 13.2) Multiple adenopatie captanti in sede mediastinica (SUVmax = 6.1).
L’intervento chirurgico si svolge in assenza di complicanze e all’esame istologico ci fornisce la diagnosi definitiva di PSEUDOCISTI TUBERCOLARE. Infatti, si evidenzia un processo infiammatorio di tipo macrofagico, con plasmacellule e linfociti T che creano delle formazioni granulomatoso-gigantocellulari con versante centrale cavitato (flogosi necrotizzante). Sia la parete cistica sia il campione di pericardio prelevato risultano negativi alla ricerca di BAAR (Bacilli Alcol Acido Resistenti) così come negativo è anche l’esame colturale. La PCR invece è positiva per il Bacillo di Koch e permette quindi di concludere per una forma localizzata di interessamento pericardico di tubercolosi extrapolmonare.
L’ecocardiogramma di controllo pre-dimissione è normale (FE 60%, minimo versamento pericardico) e il paziente viene dimesso in classe funzionale NYHA I dopo aver impostato la terapia antimicrobica in accordo con i colleghi infettivologi: prosecuzione della terapia con rifampicina/isoniazide per un totale di 12 mesi, a cui viene associata terapia con deltacortene 0.75 mg/kg/die con decalage dopo una settimana di terapia a dosaggio pieno.
Il successivo follow up clinico e strumentale risulta essere privo di eventi di rilievo.
Discussione
La pericardite tubercolare rappresenta la prima causa di versamento pericardico nei Paesi in via di sviluppo, dove rende conto di più del 90% dei casi nei pazienti con infezione da virus HIV e del 50-70% dei pazienti non HIV positivi. L’infezione può propagarsi per via ematogena, attraverso soluzioni di continuità della parete toracica oppure attraverso diffusione linfatica. Raramente l’infezione è localizzata, quando ciò si verifica in genere è coinvolta la regione del solco atrio-ventricolare destro per la presenza di linfonodi intrapericardici proprio in questa zona e il risultato è la formazione di ascessi contenenti pus e detriti cellulari.
La diagnosi definitiva di pericardite tubercolare si basa sulla dimostrazione della presenza del bacillo di Koch nel liquido pericardico o in una sezione istologica pericardica. Per i pazienti che vivono nelle aree endemiche, il trattamento anti-tubercolare empirico è raccomandato dalle Linee Guida della Società Europea di Cardiologia del 2015 nei casi di essudato pericardico, dopo aver escluso altre cause comuni. Tale approccio, invece, è controindicato nei Paesi non endemici, in cui è necessaria la diagnosi eziologica.
La complicanza più temuta è l’evoluzione della pericardite verso una forma costrittiva, la cui insorgenza è stata notevolmente ridotta grazie ai farmaci anti-tubercolari e, in casi selezionati, all’aggiunta del trattamento corticosteroideo (in pazienti non HIV positivi).
Conclusioni
Questo caso descrive una forma molto rara di coinvolgimento pericardico localizzato nella tubercolosi, in cui l’utilizzo delle tecniche di imaging di secondo e terzo livello ha permesso una diagnosi presuntiva, poi confermata dall’esame istologico della massa pseudocistica asportata durante l’intervento cardiochirurgico risolutivo.
Bibliografia
- Adler Y, Charron P, Imazio M, et al. ESC Guidelines for the diagnosis and management of pericardial diseases European Heart Journal, Volume 36, Issue 42, 7 November 2015, Pages 2921–2964
- Cosyns B, Plein S, Nuhoyanopoulos P, et al. European Association of Cardiovascular Imaging (EACVI) position paper: multimodality imaging in pericardial disease. European Heart Journal – Cardiovascular Imaging (2015) 16, 12-31
- Imazio M, Adler Y. Management of pericardial effusion. European Heart Journal (2013) 34, 1186–1197
- Mayosi BM, et al. Prednisolone and Mycobacterium indicus pranii in tuberculous pericarditis. N Engl J Med 2014;371:1121–30
- Brian D. Hoit Pericardial Effusion and cardiac tamponade in the New Millennium. Curr Cardiology Rep (2017) 19; 57
- Gulati G.S, Sharma S. Pericardial abscess occurring after tuberculous pericarditis: image morphology on computed tomography and magnetic resonance imaging. Clinical Radiology (2004) 59, 514–519
- Sung-A Chang. Tuberculous and Infectious Pericarditis. Cardiol Clin 35 (2017) 615–622